Les sténoses pulmonaires
Définition et épidémiologie
Il s’agit en fait d’un spectre étendu d’obstacle à la voie d’éjection du VD allant d’une sténose valvulaire minime n’ayant aucune conséquence à l’atrésie pulmonaire à septum intact, mortelle sans intervention.
On distingue essentiellement les sténoses valvulaires pulmonaires et les supra-valvulaires (ou des branches pulmonaires).
La sténose valvulaire pulmonaire représente 7-10% des cardiopathies congénitales et 90% des sténoses pulmonaires [2]. L’hypothèse embryologique envisage une diminution du flux sanguin au travers de la voie de sortie du ventricule droit, qui altère le développement correct de la valve pulmonaire ; les valvules vont être plus ou moins fusionnées. Les formes dites critiques sont proches d’une APSI. Les formes syndromiques sont fréquentes, essentiellement le syndrome LEOPARD ou de Noonan (dans 50% des cas de syndrome de Noonan on retrouve une sténose valvulaire pulmonaire). L’association à une rubéole congénitale ainsi que des formes familiales sont également décrites. [3]
Les sténoses supra-valvulaires et des branches pulmonaires :
Elles sont beaucoup plus rares et peuvent intéresser une partie ou toutes les branches pulmonaires. On les rencontre dans des formes syndromiques : syndrome de Williams-Beurens (hypoplasie diffuse), syndrome d’Alagille (sténoses multiples et étagées).[4] Elles peuvent être isolées ou iatrogènes (post-opératoire par exemple)
Contrairement à l’atrésie pulmonaire, le ventricule droit est bien développé mais il existe une hypertrophie ventriculaire concentrique du fait de l’obstacle. L’intégrité du septum inter-ventriculaire est un point important, modifiant l’aspect clinique, radiographique et thérapeutique de ces anomalies.
Description anatomique et variantes décrites
Dans la majorité des cas, il existe une communication inter-atriale par un foramen ovale perméable voire un ostium secondum. Cette anomalie fait presque partie intégrante de la pathologie ; elle permet par un shunt droit-gauche (responsable de la cyanose) de décharger le travail du ventricule droit.
On distingue les formes isolées de celles associées à d’autres malformations cardiaques (communication interventriculaire, tétralogie de Fallot ou ventricule droit à double issue).
La forme typique, due à une fusion des commissures avec un anneau de taille normale, est à différencier des formes dysplasiques où les valves sont dysmorphiques et l’anneau valvulaire souvent de taille réduite. Les formes dysplasiques sont l’apanage des formes syndromiques.
L’intégrité du septum interventriculaire s’associe à un développement correct des artères pulmonaires périphériques et, contrairement à l’atrésie ou sténose pulmonaire à septum ouvert, la présence de collatérales aorto-pulmonaires est très rare[3].
Clinique et évolution à long terme
Dans les formes modérées ou mineures des sténoses valvulaires pulmonaires les patients restent asymptomatiques pendant plusieurs décennies. Elles peuvent être découvertes fortuitement ou être responsable d’une dyspnée d’effort, d’une érythrose faciale et d’une acrocyanose. Le traitement par cathétérisme seul n’est réalisé que dans le but de préserver la fonction ventriculaire droite ou pour réaliser la fermeture d’une CIA. La survie est identique à celle de la population générale.[2]
Les formes sévères, dites critiques, ont une révélation néonatale, avec apparition rapide d’une cyanose. La cyanose est due à un shunt droit-gauche à travers une communication inter-auriculaire. Cette forme est ductodépendante et nécessite un traitement rapide pour lever l’obstacle.[3] Après traitement par dilatation au ballonnet, la diminution du gradient est immédiate et les complications immédiates sont rares. Le principal risque est la récidive qui survient dans environ 10% des cas.[5] Comparativement, les patients traités chirurgicalement présentent moins de récidive mais la morbidité opératoire est plus importante et le pronostic est grevé par l’apparition dans 30% des cas d’une insuffisance pulmonaire. Néanmoins le pourcentage de réintervention à long terme est moindre que pour le cathétérisme.[6] Une étude estime la survie à 25 ans à 93% après traitement chirurgical.[7] Le pronostic, quelle que soit la technique employée, est bon, avec une qualité de vie satisfaisante.[5,6,7]
Quant aux sténoses entrant dans le cadre d’un syndrome de Williams-Beurens, l’évolution est favorable dans la majorité des cas, et une attitude abstentionniste est souvent choisie.
Traitement
Le développement des techniques de cathétérisme interventionnel décrit dans les années 80 par Kan a révolutionné la prise en charge de cette malformation.
En effet, initialement, seul un traitement chirurgical était envisageable.
La technique consiste à introduire par voie vasculaire un ballonnet expansible au niveau de la sténose. L’indication est retenue pour des mesures de gradient pic à pic supérieures à 50 mmHg. La taille du ballonnet est choisie en fonction de la taille de l’anneau valvulaire avec comme proportion un ratio 1,2-1,3 voire plus en cas de valve dysplasique.[5]
Le traitement chirurgical est aujourd’hui réservé aux formes dont le cathétérisme n’est pas venu à bout ou qui entre dans le cadre de cardiopathie complexe.
Les sténoses des branches pulmonaires, quand elles entrainent un retentissement sur la fonction ventriculaire droite, peuvent être traitées par dilatation au ballonnet avec éventuelle mise en place de stent ( technique controversée en raison du risque de thrombose et d’absence de croissance possible).
Imagerie
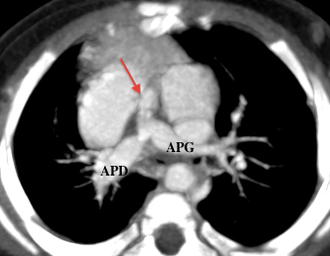
Lorsque le septum interventriculaire est intact, l’imagerie en coupes n’a que peu d’interêt. En effet, l’échographie est largement suffisante dans la quasi totalité des cas. Le traitement, quand il est nécessaire, est souvent réalisé par cathéterisme cardiaque, ce qui permet une première phase diagnostique d’étude précise de la ou des sténoses ainsi que leur retentissement hémodynamique. En post-intervention, la surveillance échographique est nécessaire mais largement suffisante et les techniques d’imagerie en coupes n’interviennent pas.
Néanmoins, lorsqu’il existe une CIV associée, la recherche de collatérales aorto-pulmonaires par l’angioTDM ou l’angioIRM pulmonaire est très utile et permet de dépister celles-ci avec une grande précision [8] quant à l’anatomie, la taille, les confluences, et ce de manière non invasive.
Le scanner permet également de guider un geste de dilatation par cathétérisme de manière fiable [10] et de montrer les sténoses périphériques comme dans le syndrome de Williams-Beurens[11].
Il faut souligner que les sténoses peuvent être surestimées en IRM [9]

Bibliographie
- Brock RC, Campbell M. Valvulotomy for pulmonary valvular stenosis. Heart. 1950 ; 12(4) : 377-402
- Boudjemline Y. Sténoses et atrésies pulmonaires à septum interventriculaire intact. EMC Cardiologie. 2011 ; :11-940-D-90
- El Louali F, Villacampa C, Aldebert P, Dragulescu A, Fraisse A. Sténose pulmonaire et atrésie pulmonaire à septum interventriculaire intact. Archives de pédiatrie.2011 ;18 : 331-337
- Baum D, Khoury GH, Ongley PA, Swan HJ, Kincaid OH. Congenital stenosis of the pulmonary artery branches. Circulation. 1964 ; 29 : 680-687
- Rao PS. Percutaneous balloon pulmonary valvuloplasty : state of the art.Cathererization and cardiovascular interventions.2007 ; 69 :747-763
- Peterson C, Schilthuis JJ, Dodge-Khatami A, Hitchcock JF, Meijboom EJ, Bennink WE. Comparative long-term results of surgery versus ballon valvuloplasty for pulmonary valve stenosis in infants and children. Ann Thorac Surg.2003 ; 76 : 1078-83
- Roos-Hesselink JW, Meijboom FJ, Spitaels SE, vanDomburg RT, vanRijen EH, Utens EM, Bogers AJ, Simoons ML. Long-term outcome after surgery for pulmonary stenosis (a longitudinal study of 22-23 years). Eur Heart Journal. 2006 ; 27 : 482-488
- Srinivas B, Patnaik AN, Rao PS. Gadolinium-enhances three-dimensional magnetic resonance angiographic assesment of the pulmonary artery anatomy in cyanotic congenital heart disease with pulmonary stenosis or atresia : comparison with cineangiography. Pediatr Cardiol. 2011 ; 32 : 737-742
- Strouse PJ, Hernandez RJ, Beekman RH. Assesment of central pulmonary arteries in patients with obtructive lesions of the right ventricle : comparison of MR imaging and cineangiography. AJR. 1996 ; 167 : 1175-1183
- Greil GF, Kuettner A, Schoebinger M, Meinzer HP, Claussen CD, Hofbeck M, Sieverding L . Visualization of peripheral pulmonary artery stenosis using high-resolution multidetector computed tomography.Vasc Med 2005 10: 235
- Park JH, Kim HS, Jin GY, Joo CU, Ko JK.. Demonstration of peripheral pulmonary stenosis and supravalvular aortic stenosis by different cardiac imaging modalities in a patient with Williams syndrome — usefulness of noninvasive imaging studies International Journal of Cardiology. 2008 ; 128 :e95–e97