Canal atrioventriculaire
Définition et épidémiologie
Les anomalies du septum atrioventriculaire concernent un spectre de malformations comprenant une jonction atrioventriculaire commune associée à un déficit de la septation atrioventriculaire.
Ces anomalies représentent 4% des cardiopathies congénitales, la prévalence varie entre 0,24/1000 à 0,31/1000 des naissances[1].
Il existe un lien étroit entre ces malformations et la trisomie 21, puisque 20% voire plus des patients atteints de trisomie 21 présentent une telle malformation, et la présence d’une trisomie 21 est retrouvé dans un tiers des patients ayant une anomalie de la jonction atrioventriculaire [1,2].
La trisomie 18, le syndrome d’Ellis-Van- Creveld ou le syndrome de Pallister-Hall sont également fréquemment associés[1].
Ces anomalies comportent donc à des degrés différents : une CIA type ostium primum, une CIV périmembraneuse du septum d’admission, des anomalies des valves auriculoventriculaires et un anneau atrioventriculaire unique.
Embryologie
Ces anomalies sont également nommées anomalies des bourgeons endocardiques. Cette dénomination rend compte de leur origine embryologique. En effet, la jonction atrioventriculaire provient du développement des bourgeons endocardiques. Un défaut de signal de différenciation des cellules endocardiques en cellules mésenchymateuses est à l’origine d’un défaut de la formation des valves auriculoventriculaires ainsi que du septum membraneux interventriculaire. Le septum interauriculaire est également atteint, le septum primum (excroissance endocardique du toit de l’oreillette primitive) se développe insuffisamment, à l’origine d’une CIA type ostium primum.[3]
Description anatomique et variantes
Le canal atrioventriculaire commun complet : (67%)

Il associe :
- une CIA type ostium primum : CIA au niveau de la partie inférieure du septum interauriculaire juste en amont de la valve atrioventriculaire
- un anneau atrioventriculaire commun : contrairement au cœur normal, il existe une seule valve atrioventriculaire commune aux deux ventricules
- des anomalies des valves auriculoventriculaires : la valve unique surplombe les deux ventricules, elle comporte 5 feuillets :
un grand feuillet antéro-supérieur traversant le septum interventriculaire (SIV)
un feuillet postéro-inférieur traversant également le SIV
un feuillet latéral droit
un feuillet postérieur droit
un feuillet latéral gauche
- La chambre de chasse du VG est allongée par un bombement de la valve antérieure dans la voie d’éjection, donnant l’aspect angiographique caractéristique en « col de cygne » de la chambre de chasse du VG.
Le rapport de longueur chambre de chasse VG/ chambre de remplissage VG normalement égal à 1, augmente.
La principale classification utilisée, bien qu’imparfaite a été décrite par Rastelli [4], elle distingue 3 types de CAV complets différents, en fonction de la morphologie et des insertions valvulaires du feuillet commun antérieur :
- Typa A : feuillet antérieur adhérent au ventricule gauche et attaché à la crête du septum interventriculaire
- Type B : feuillet antérieur présentant une attache au ventricule droit par un muscle papillaire anormal
- Type C : feuillet antérieur flottant, non relié au septum interventriculaire

FLD: feuillet latéral droit
FPD: feuillet postérieur droit
FA: feuillet antéro-supérieur
FPI: feuillet postéro-inférieur
FLG: feuillet latéral gauche
Le type A est souvent associé à une obstruction de la voie d’éjection du VG. Le type B est le plus fréquent et le type C est souvent associé à d’autres anomalies cardiaques (tétralogie de Fallot, coarctation aortique, ventricule droit dominant).
Les formes isolées, sans autres anomalies, sont l’apanage des trisomies 21[3].
Le canal atrioventriculaire commun partiel : (25%)
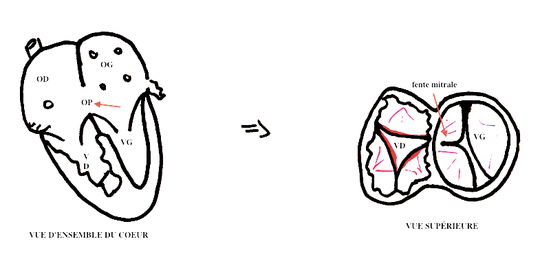
Il associe :
- la présence d’un ostium primum
- une fente de la grande valve mitrale
- un anneau auriculoventriculaire mais deux orifices auriculoventriculaires distincts (séparés par une languette fibreuse)
- un septum interventruclare intact
La valve tricuspide est habituellement intacte mais la valve mitrale présente un aspect trifolié par une fente sur la grande valve.
CAV intermédiaire : (8%)
Il existe une languette fibreuse formant deux orifices atrioventriculaires mais celle-ci n’est pas rattachée au septum interventriculaire formant ainsi une CIV d’admission restrictive.
Physiopathologie
- Shunts dits « facultatifs » : shunt gauche-droit à travers la CIA et la CIV
- Shunts dits « obligatoires » : VG-OD= responsable d’une dilatation de l’oreillette droite
VD-OG= responsable d’une cyanose discrète
Shunts majoritairement gauche-droit= augmentation des pressions ventriculaires droites= hypertension artérielle pulmonaire.
Clinique
CAV complet
L’histoire naturelle est sombre avec selon les auteurs quasiment 100% de mortalité à 1 ou 2 ans. Les symptômes débutent dans les premiers mois de vie par une cyanose et des signes de défaillance cardiaque droite, évoluant vers une maladie vasculaire pulmonaire fixée, en raison de la surcharge droite.
CAV partiel
La clinique d’un CAV partiel ressemble à celle d’une simple CIA, sauf s’il existe une insuffisance mitrale importante associée. Sans intervention, l’espérance de vie est courte, aux alentours des 40 ans. Mais avec les progrès de la chirurgie, l’espérance de vie est largement augmentée
Traitement
CAV complet
- Equilibré :
Seul le traitement chirurgical permet d’améliorer la survie.
Dans les premiers mois de vie, avant l’apparition d’une maladie vasculaire pulmonaire irréversible.
Il consiste
- sous CEC,
- par une transatriotomie droite,
- à fermer le defect septal auriculaire et ventriculaire par un ou deux patchs péricardiques selon les équipes.
Par ailleurs, une plastie de la valve mitrale est effectuée par suture de la partie gauche du feuillet antérieure et du feuillet postérieur.
- Présence d’un ventricule hypoplasique ou d’un straddling d’un cordage
Dans la majorité des cas, le ventricule droit est dominant. L’option chirurgicale sera donc celle d’une réparation univentriculaire, aboutissant à une dérivation cavopulmonaire totale.
CAV partiel
Le traitement chirurgical est effectué plus tard dans la petite enfance, par une suture de la fente mitrale et une fermeture de l’ostium primum par un patch péricardique.
Evolution à long terme
La mortalité peropératoire est de l’ordre de 3% de nos jours [5]; les principales complications à long terme sont une insuffisance mitrale ou une sténose de la voie de sortie gauche. Cela mène à une réintervention dans environ 10% des cas. Les formes nécessitant une réintervention ont un moins bon pronostic.
Imagerie
Préopératoire
L’échocardiographie est le gold standard en pré-opératoire de ces anomalies.
Le scanner et l’IRM n’ont pas de place en pratique.
L’RM est capable de détecter avec précision l’anatomie lésionnelle mais n’est pas indiquée car l’échographie fournit les informations préopératoires nécessaire. L’IRM ou le scanner sont limités par la mauvaise évaluation de l’anatomie valvulaire et des muscles papillaires[8, 9, 10].
L'IRM peut être utile pour déterminer avec précision les volumes ventriculaires, surtout dans les formes complètes déséquilibrées. Il permet également de préciser l’anatomie du septum interventriculaire d’admission, le défect septal étant parfois difficile à voir en échographie dans les cas où de multiples cordages de la valve antérieure s’insèrent dessus; une séquence ciné en 4 cavités visualise alors le jet du shunt.[8]
Il faut analyser avec précision le situs, l’anatomie de l’arbre trachéo-bronchique, les isomérismes étant fréquemment associés.
L’analyse de la voie de sortie gauche est également intéressante, car elle peut etre atteinte.

Post-opératoire
L’IRM ou le scanner n’ont pas de place dans cette pathologie, l’échographie est largement suffisante.
Dans le cas particulier des formes déséquilibrés, après dérivation cavopulmonaire partielle ou complète, l’intérêt de l’imagerie en coupes rejoint celui de l’évaluation post-opératoire des ventricules uniques fonctionnels.
GALERIE D'IMAGES:
Bibliographie
- Craig B. Atrioventricular septal defect : from fetus to adult. Heart. 2006 ; 92 : 1879-1885
- Bassil Eter R., Roux D. Canal atrioventriculaire. EMC Cardiologie. 2008 ; 11-940-C-40
- Calabro R, Limongelli G. Complete atrioventricular canal. Orphanet Journal of Rare Diseases.2006 ; I : 8
- Rastelli GC, Kirklin JW, Titus JL. Anatomic observations on complete form of common atrioventricular canal with special reference to atrioventricular valves. Mayo Clinic Proc. 1966 ; 41 :296
- Manning PB. Partial atrioventricular canal : Pitfalls in technique. Semin Thorac Cardiovasc Surg Pediatr Card Surg Ann. 2007 ; 10 : 42-46
- Crawford FA, Stroud MR. Surgical repair of complete atrioventricular septal defect. Ann Thorac Surg. 2001 ; 72 : 1621-9
- Hoohenkerk G. J.F., Bruggemans E.F., Koolbergen D.R., Rijlaarsdam M.E.B., Hazekamp M.G. Long-term results of reoperation for left atrioventricular valve regurgitation after correction of atriventricular septal defects. Ann Thorac Surg. 2012 ; 93 : 849-55
- Parsons JM, Baker EJ, Anderson RH, Ladusans EJ, Hayes A, Qureshi SA, Deverall PB, Fagg N, Cook A, Maisey MN, Tynan M. Morphological evaluation of atrioventricular septal defect by magnetic resonance imaging. Heart J. 1990 ; 64 : 138-145
- Jacobstein MD, Fletcher BD, Goldstein S, Riemender TA. Evaluation of atrioventricular septal defect by magnetic resonance imaging. Am J Cardiol. 1985 ; 55 : 1158-61